.

- HOME
- 研究概要(教授メッセージ)
- 研究内容
| 細胞接着性タンパク質(フィブロネクチン・コラーゲンなど)の細胞接着活性を有する部分のアミノ酸配列(Arg-Gly-Asp-Ser : RGDS)のみを人工的に作り、他のペプチドや高分子と組み合わせて細胞が接着・増殖しやすい人工の足場を作る。そして、細胞や動物実験でその有用性を評価する。 | 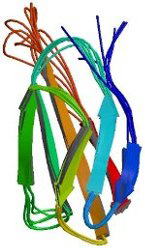 |
(スローリリース用DDS担体の合成)
海藻由来の天然多糖であるアルギン酸を再生医工学用足場として利用できるように、生理活性ペプチドと組み合わせ細胞と親和性の高い足場を合成する。
また、同様にアルギン酸と生理活性ペプチドとを組み合わせ、増殖因子などのタンパク質がスローリリースできるようなDDSの担体の合成をおこなう。
| ペプチドの2次構造であるα-ヘリックス、β-シート構造を人工的にデザインし、それらの構造を集積化することにより、新規のペプチド由来のナノファイバーを代表とする構造体を構築する。 |  |
ペプチドを用いて、細胞凝集塊(スフェロイド)の作製技術を確立する。
(生体高分子と合成高分子のハイブリッドによる高機能化)
合成高分子表面に細胞接着活性を有するアミノ酸配列(Arg-Gly-Asp-Ser : RGDS)を人工的に作り、化学的に固定化することにより、細胞と親和性の高い材料表面を作る。そして、培養細胞を用いてその有用性を評価する。
タンパク質や多糖類を合成高分子表面に化学固定し、生体適合性を有する材料を作る。また、水溶性合成高分子と組み合わせて、機能性を持ったゲルを作る。
高分子や金属、セラミックスなど、医療用デバイスの構成材料として用いられているバイオマテリアルの表面を、非天然アミノ酸や人工ペプチド・タンパク質によって修飾することで生理活性(例えば、抗血栓性や細胞接着性)を付与する新しい方法を開発する。
| 細胞増殖因子やその他の機能性タンパク質の活性部位は、アミノ酸配列にして10残基ほどである。それらの配列を人工的に化学合成し、水溶性高分子とハイブリッドすることにより、天然と同等の活性発現が得られるような分子を設計し合成する。 | 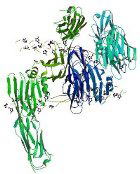 |
タンパク質中にプロリン残基を含み同じ配列が周期的に繰り返されている周期性タンパク質が、多数発見されている。しかしながら、それらの機能・構造については明らかにされていない。そこで。Xaa-ProやXaa-Yaa-Proを繰り返し単位とするポリペプチドを合成し、それらの構造や機能を実験科学的に解明する。
組織工学用の足場材料や組織置換型医療デバイスの基材としての利用を志向し、細胞外マトリクスを模倣した人工タンパク質やペプチド、もしくはそれらと合成高分子との複合体を、化学的手法と遺伝子工学的手法を駆使して合成する。
増殖因子の生理活性配列だけを切り出したペプチドは、タンパク質中に存在する場合とは違って特定の高次構造を形成できないため、その生理活性は極めて低い。そこで、分子動力学計算などによる高次構造(二次構造)予測と化学合成を組み合わせることで、より緻密にネイティブの増殖因子を模倣したペプチドの創製を目指す。
.
Copyright © 2011 HIRANO Yoshiaki. All Right Reserved.